
 发布时间:2024/03/20 点击数:560
发布时间:2024/03/20 点击数:560 01 关于AKITA
总部设在芬兰,奥卢的器官芯片制造商AKITA,by Finnfadvance,成立于2019年。
搭载高通量器官芯片板,可被设计成单器官和多器官,兼容多种成像模式,高人体相关性的下一代人体体外模型,加速药物开发,降低临床前试验失败的风险,也可用于个性化医疗。
上海曼博生物医药科技有限公司是AKITA,by Finnfadvance官方授权的中国经销商。
02 AKITA Plate
AKITA Plate,超.高通量的器官芯片板(图1),可设计成单器官和多器官(图2),旨在提供微生理学培养条件,以生成和维持生物屏障(图3),包括血脑屏障、气道屏障、肠道上皮屏障和血管内皮屏障等。

图1:AKITA Plate的两种尺寸
(96孔板 & 384孔板)
1)96孔格式:允许进行更高体积 (150uL) 的实验,每板可进行24个重复;2)384孔格式:允许进行更高通量,96个实验,但体积较小 (30uL)。
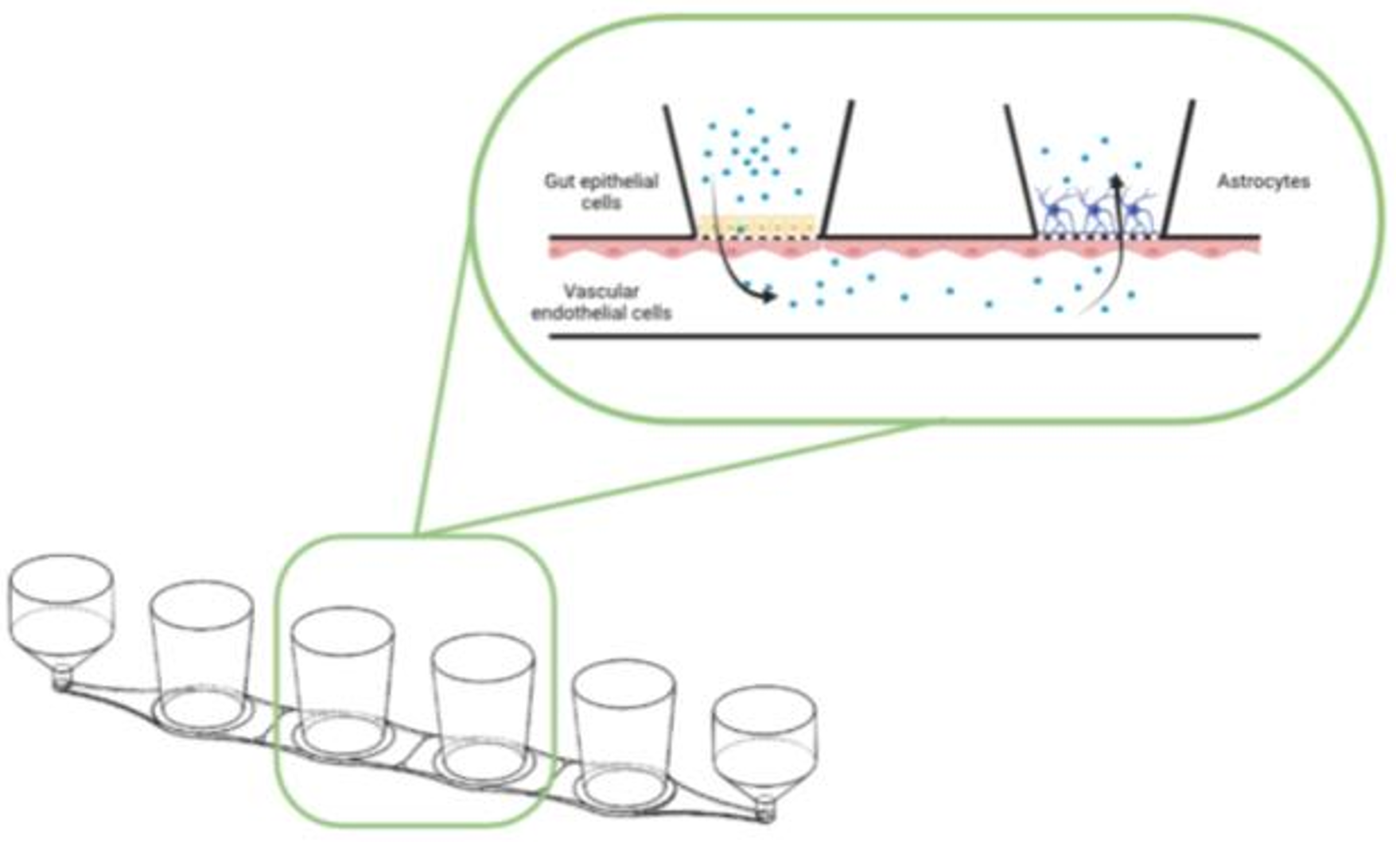
图2:AKITA多器官连接
2-6个连接和血管化组织,每块96孔板10-24次多器官测试,图中以肠-神经双器官为例。
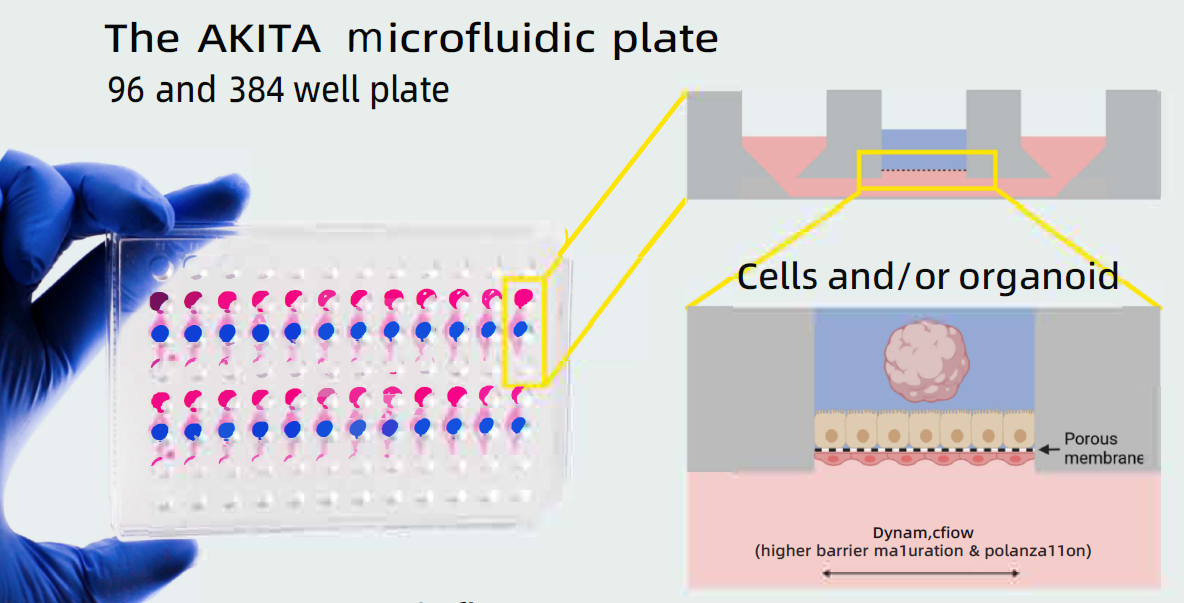
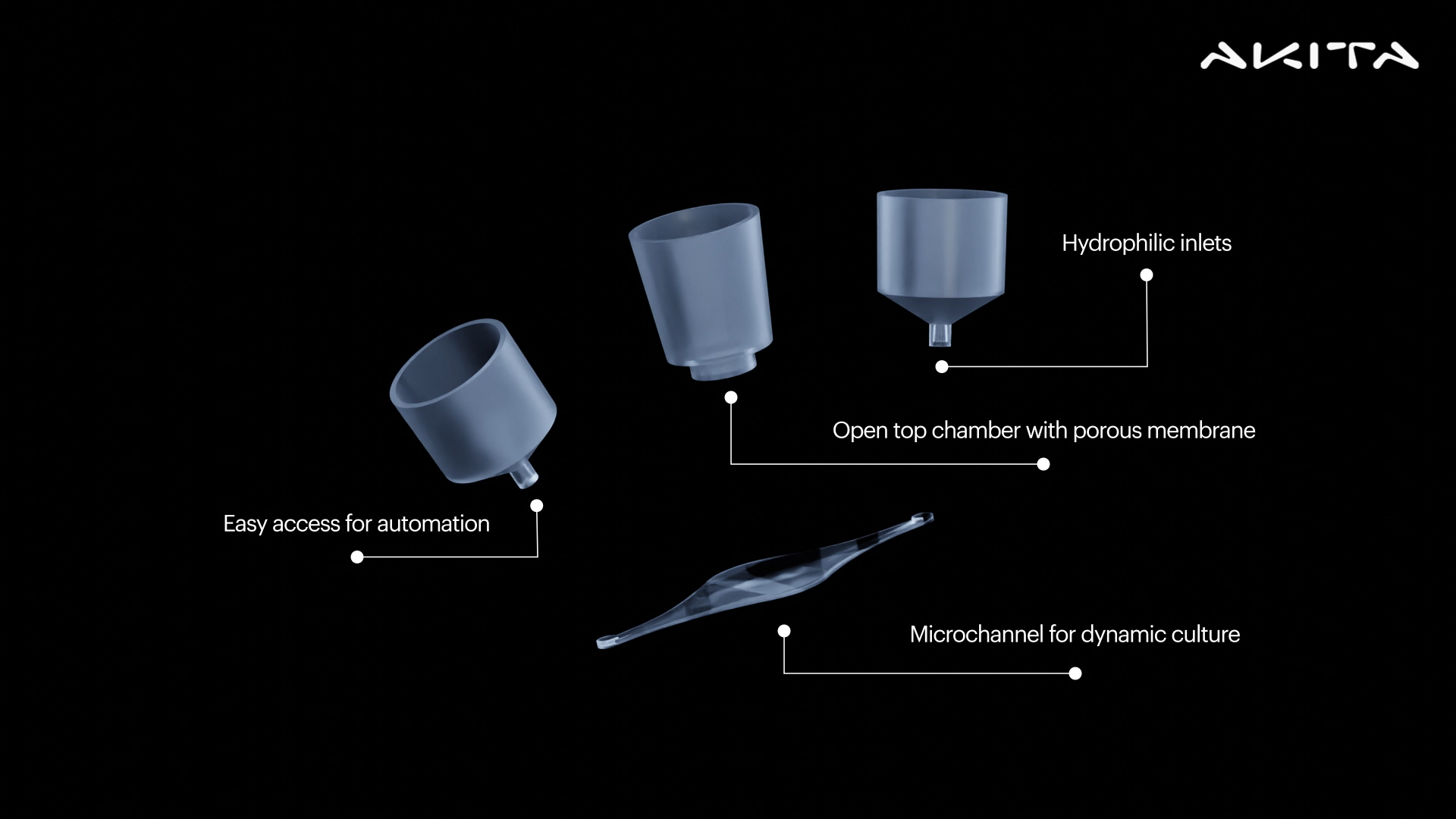
图3:类似体内条件,内皮细胞在持续的流动条件下维持,上皮细胞则以静态方式维持,可是浸没状态或气液界面状态下,中间腔室也可放与培养的类器官甚至肿瘤组织。
AKITA Plate允许高分辨率和高内涵成像(图4),属于用户友好型器官芯片平台,兼容几乎所.有成像模式:数字全息术、超声成像、电子显微镜、共焦成像,包括MRI,具有SBS标准。
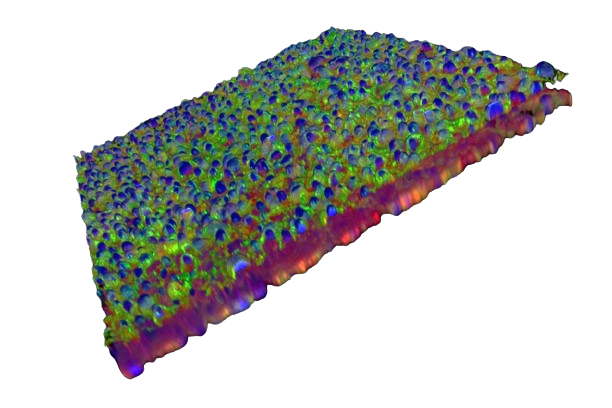
图4:AKITA Plate 高分辨率成像
03 AKITA Lid
AKITA Lid是一款以客户便捷性为前提考虑因素的4电极TEER仪器。完全无线控制和监控使得数据收集和远程监测一步到位。
多个Lid可以同步使用,提供大型实验的概览,使其成为真正的高通量筛选和高内涵筛选(HTS和HCS)准备系统。
与AKITA Lid兼容,各样本几秒钟内同时完成跨膜电阻(TEER )的测量,并支持连续长期测量(图5)。

图5:AKITA Lid
AKITALid是专为AKITA Plate设计的多通道TEER(经上皮电阻)测量装置。电学读数速度快,可根据需要进行重复测量。
TEER(经上皮电阻)值测量,是快速和可重复分析评估生物屏障完整性所需的更可靠的非光学测量技术。
04 AKITA Rocker
无泵流体操作平台,平稳的摇摆动作可通过AKITA Plate的微通道进行连续培养基灌流。
摇摆角度和摇摆速率均可控,允许用户设置特定于模型的条件,适用于任.何标准的细胞培养箱,无论气体、湿度和温度要求如何。

图6:AKITARocker
AKITARocker经过优化且兼容原装芯片的设备完成类器官芯片研究设置,同时运行4块AKITA Plate,用户可通过软件远程操控。
05 结语
作为一种更快、更精确、可重复的药物研究和开发系统,对于靶向人体特定受体或免疫系统的治疗手段效果更好,如CAR-T细胞治疗或者基因治疗,可桥接传统的体外2D模型和体内模型间的鸿沟。目前AKITA已被AstraZeneca等知.名药企充.分验证,应用范围广.泛(图7)。

图7:AKITA的应用领域及成熟器官模型速览
* 关注我们,更多AKITA资讯敬请期待!欢迎咨询获取更多产品资料~


 MineBio 精选
MineBio 精选  BioLamina人类重组层粘连蛋白
BioLamina人类重组层粘连蛋白 














